
Anvisa recebe pedido de uso emergencial do Butatan
Pedido foi enviado à Agência na manhã desta sexta-feira (8). Prazo para análise é de dez dias caso não haja dúvidas sobre documentos.

Pedido foi enviado à Agência na manhã desta sexta-feira (8). Prazo para análise é de dez dias caso não haja dúvidas sobre documentos.

A análise dos resultados dos estudos clínicos será feita continuamente. Medida vale apenas para vacinas contra a Covid-19.

A Agência Nacional de Vigilância Sanitária (Anvisa) publicou, na última terça-feira (17/11), no Portal Brasileiro de Dados Abertos e na plataforma Gov.br informações relacionadas à
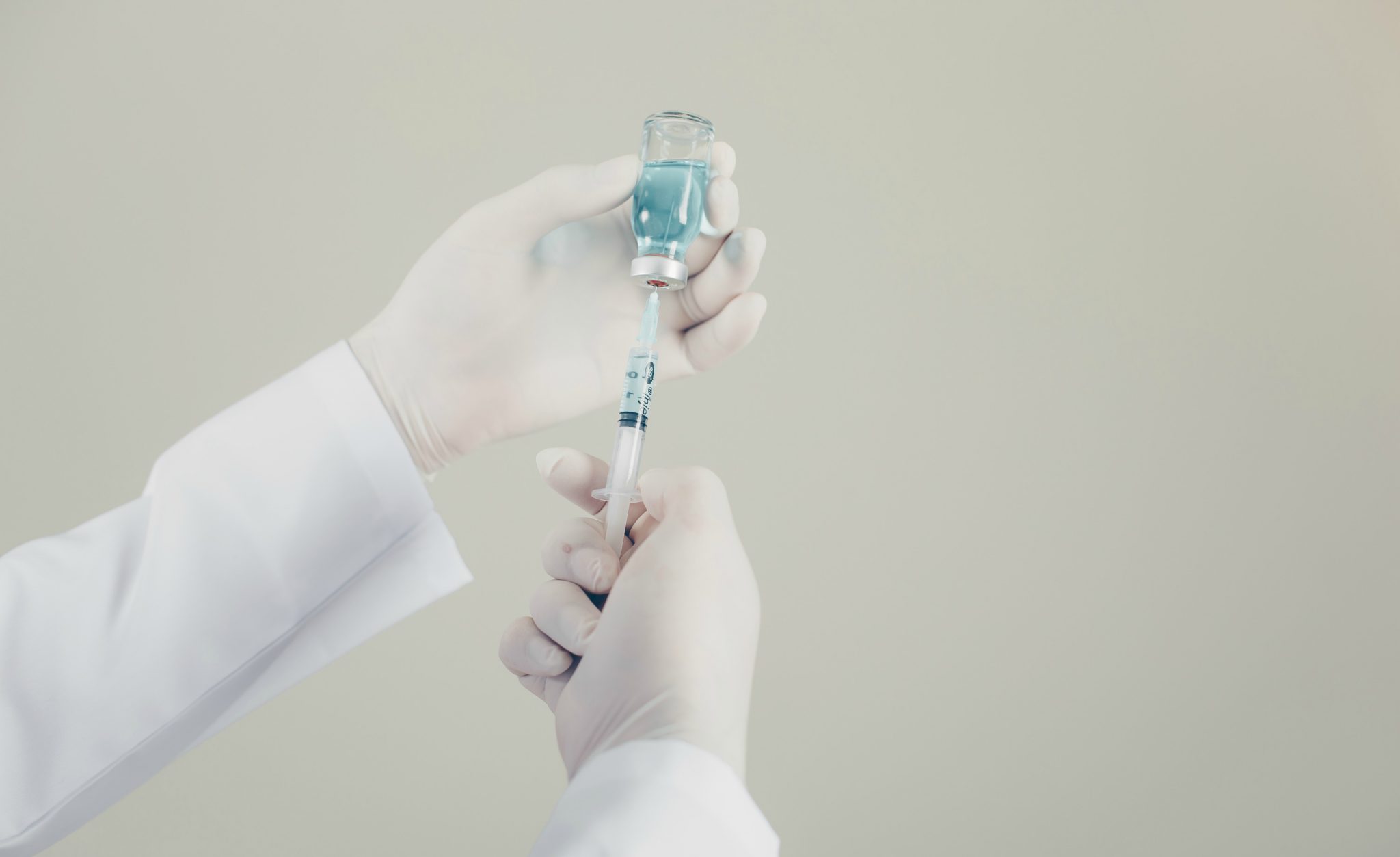
Agência revelou em nota que não divulgou a natureza do evento adverso que causou a pausa nos estudos clínicos em respeito à privacidade dos voluntários.

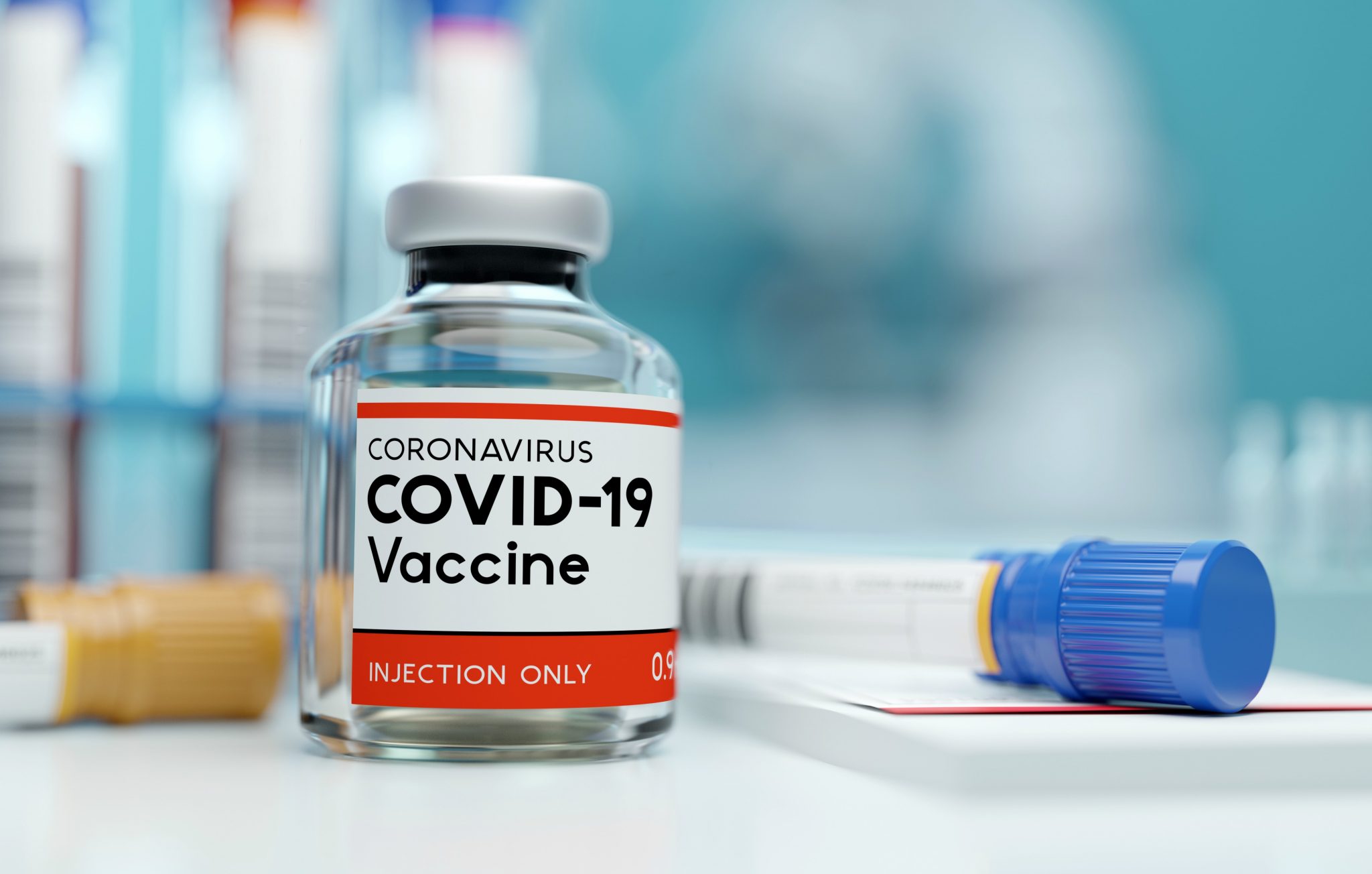
Processo tem como objetivo criar agilidade regulatória quando os pedidos de registro das vacinas no Brasil acontecerem.

A decisão fui publicada pela Agência nesta quinta-feira (24/9), por meio de uma nova resolução, a RDC nº 425/2020.
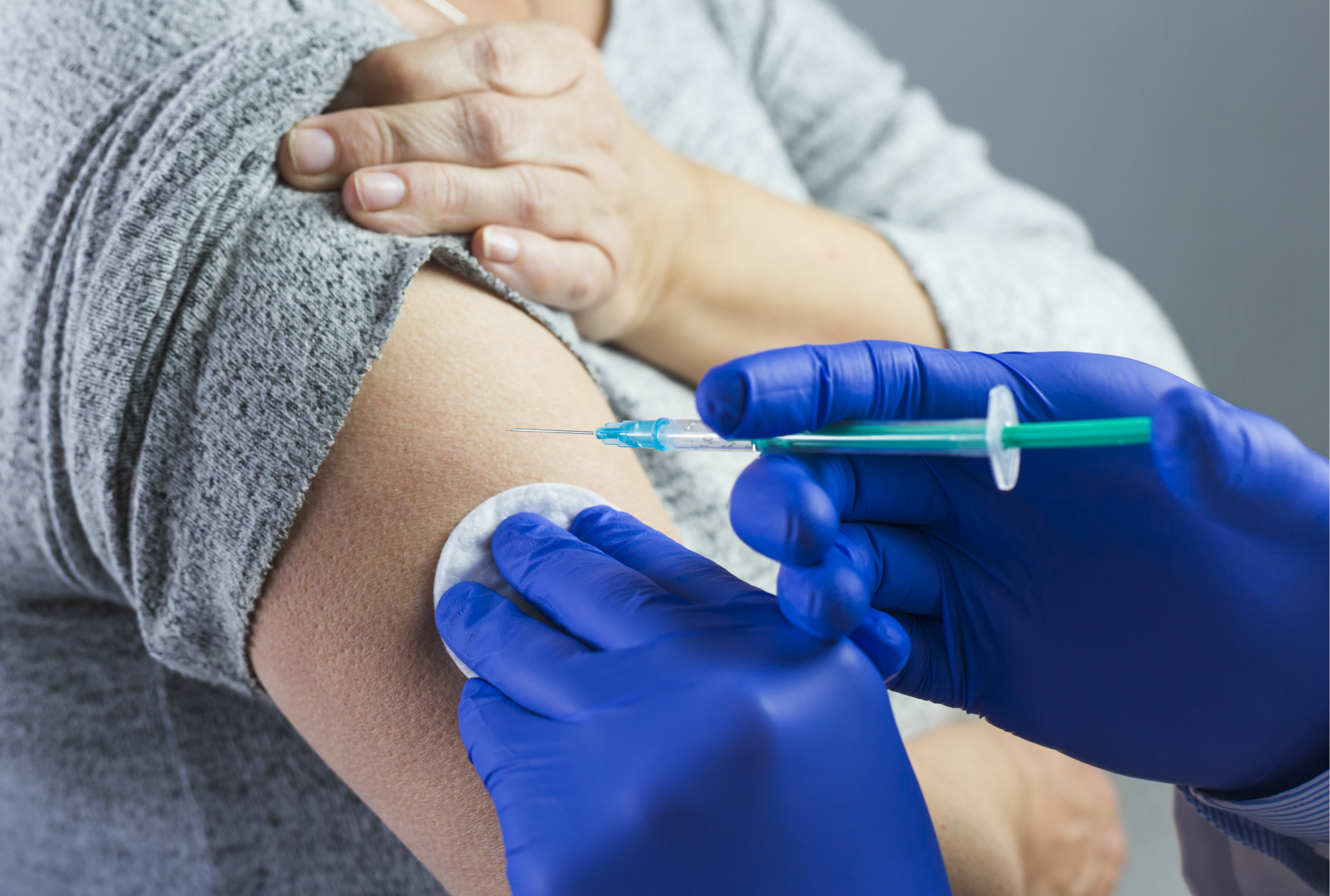
Entre as mudanças autorizadas, estão a ampliação do número de participantes no Brasil e também da faixa etária.
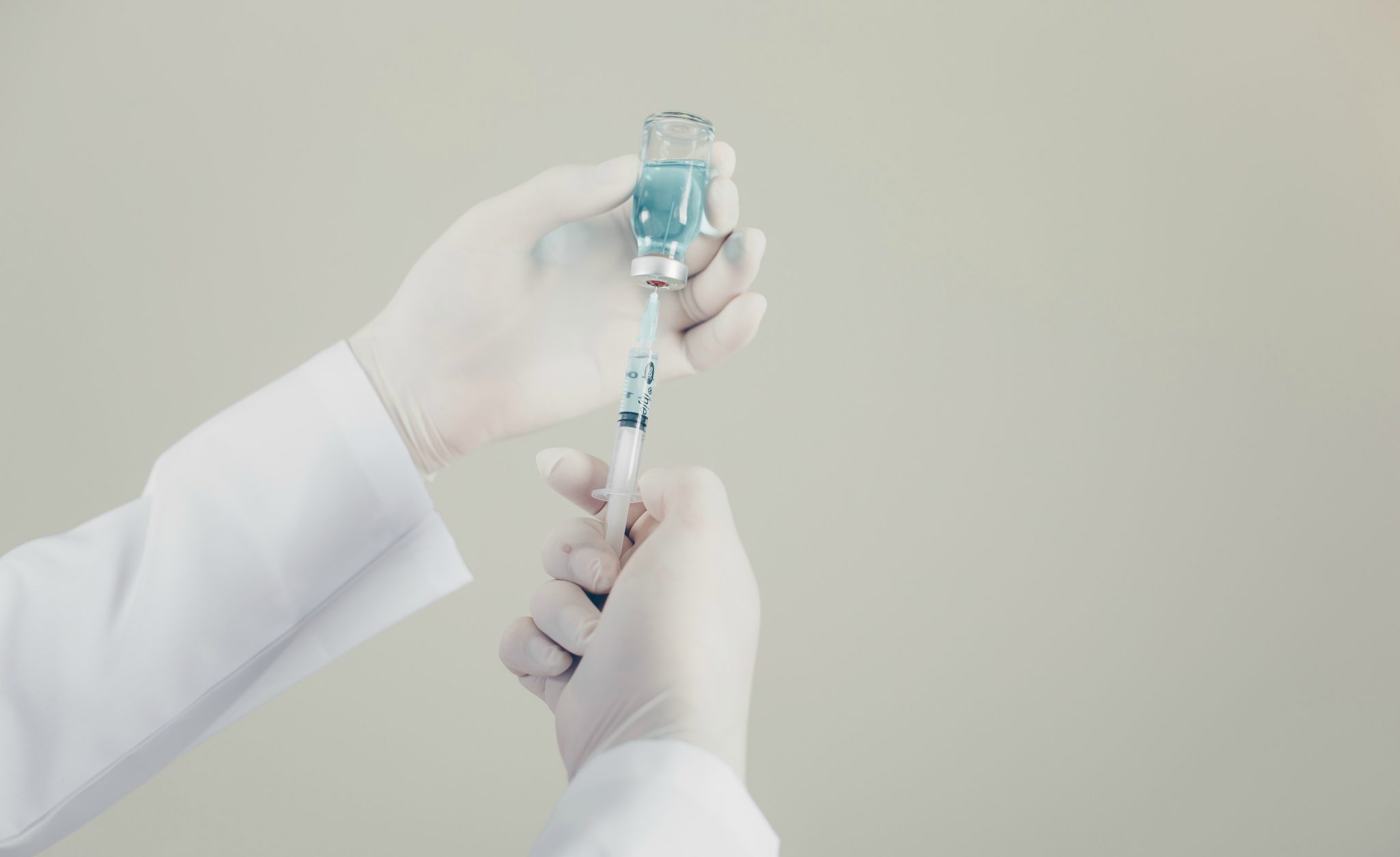
Autorização para retomada foi dada pela Anvisa no último sábado (12), após AstraZeneca entrar em contato oficialmente.

Para notícias e ofertas exclusivas, digite seu e-mail abaixo.
Para notícias e ofertas exclusivas, digite seu e-mail abaixo.
Utilizamos cookies para garantir que você tenha a melhor experiência em nosso site. Se você continuar a usar este site, vamos assumir que você está feliz com isso.