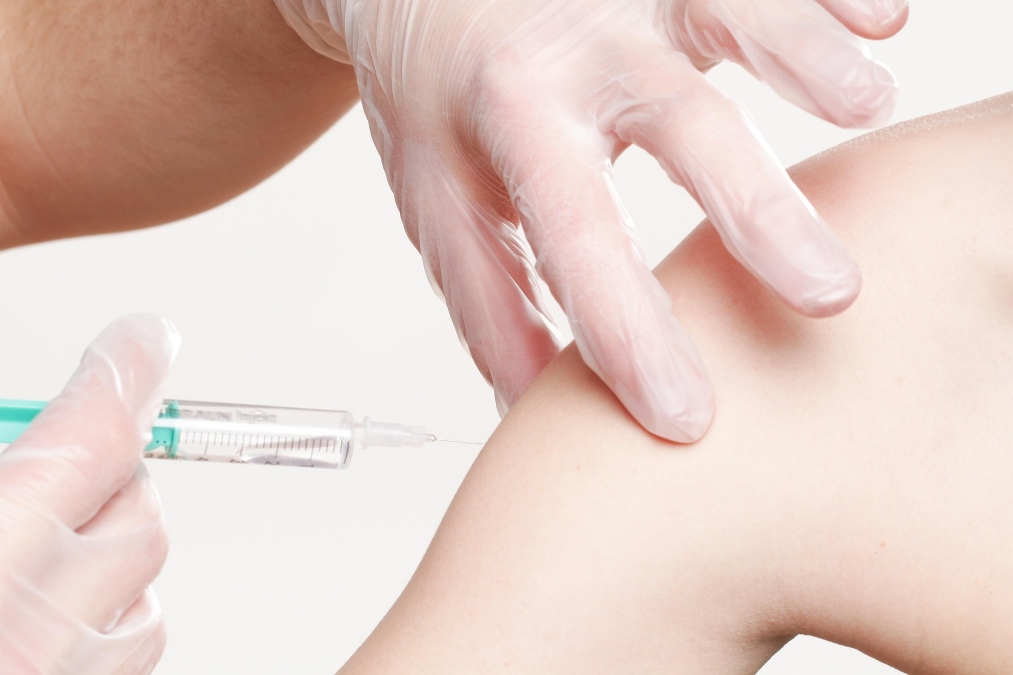
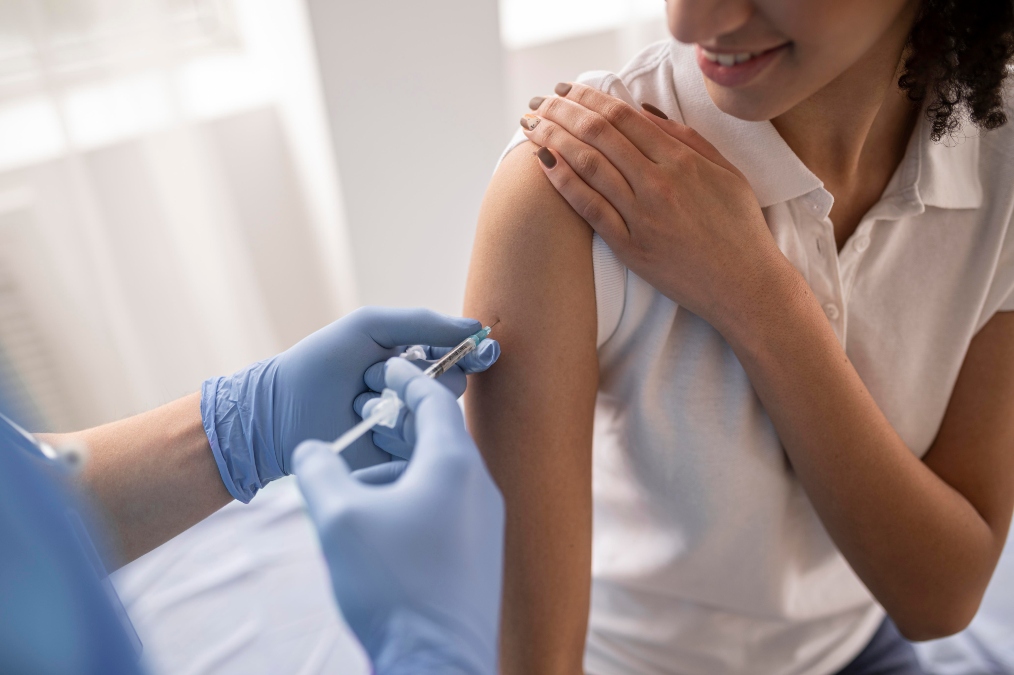
A Gilead Sciences Brasil anuncia que a Agência Nacional de Vigilância Sanitária (Anvisa) aprovou o registro do lenacapavir para duas indicações:
- Profilaxia pré-exposição (PrEP) para reduzir o risco de HIV-1 sexualmente adquirido em adultos e adolescentes acima de 12 anos pesando pelo menos 35 kg que correm o risco de adquirir o HIV-1;
- Tratamento de pacientes multiexperimentados (HTE) com HIV-1 resistente a múltiplas classes de antirretrovirais.

Com estas autorizações, o lenacapavir se torna o primeiro inibidor de capsídeo aprovado no Brasil e a primeira PrEP injetável de aplicação semestral disponível no país, unindo inovação científica tanto para prevenção quanto para o manejo de casos complexos de resistência viral.
As submissões regulatórias foram protocoladas pela empresa em novembro de 2024 (HTE) e março de 2025 (PrEP), ambas avaliadas pela Anvisa sob análise prioritária, dada a relevância epidemiológica e o potencial impacto em saúde pública.
“As aprovações do lenacapavir para PrEP e para pacientes multiexperimentados representam um marco para a resposta ao HIV no Brasil. Trata-se de uma inovação de longo prazo que amplia opções de prevenção e oferece esperança para pessoas com resistência extensa e opções terapêuticas restritas. A Gilead está comprometida com a colaboração contínua com autoridades, especialistas e a comunidade para ampliar o impacto positivo dessas duas novas indicações”, afirma André Abrahão, Diretor Médico da Gilead Sciences Brasil.
Potencial avanço na prevenção: aprovação para PrEP
A aprovação da indicação para PrEP é sustentada pelos ensaios clínicos globais de Fase 3 PURPOSE 1 e PURPOSE 2. Nos estudos, o lenacapavir demonstrou eficácia para prevenção para infecção pelo HIV igual ou superior a 99,9%, com:
- Nenhuma infecção entre participantes que receberam o medicamento no PURPOSE 1;
- Apenas 2 infecções em 2.179 participantes no PURPOSE 2;
Os resultados demonstraram superioridade em relação à PrEP oral diária (entricitabina + fumarato de tenofovir desoproxila). A aplicação semestral foi associada a altos níveis de adesão, persistência e satisfação, especialmente entre jovens, pessoas vulneráveis e indivíduos com dificuldades para manter o uso diário de comprimidos.
Esta aprovação amplia significativamente o portfólio de prevenção disponível no Brasil e tem o potencial de fortalecer a estratégia de prevenção combinada adotada pelo Ministério da Saúde.
Avanço no tratamento: aprovação para pacientes HTE
Para a indicação de tratamento, o registro do lenacapavir é fundamentado nos resultados do estudo CAPELLA (Fase 3), conduzido com pacientes multiexperimentados (HTE), caracterizados por resistência extensa e múltiplas falhas terapêuticas.
No estudo, 88% dos participantes que receberam lenacapavir associado a um regime otimizado alcançaram supressão viral (<50 cópias/mL) após 26 semanas. O medicamento se torna, assim, uma alternativa inovadora para um grupo específico de pessoas vivendo com HIV com opções extremamente limitadas de tratamento.
Leia também: Anvisa aprova nova RDC que regulamenta o receituário eletrônico de medicamentos controlados
A administração semestral do lenacapavir, associado a um regime otimizado, representa uma opção terapêutica diferenciada e facilita o manejo clínico em casos complexos.