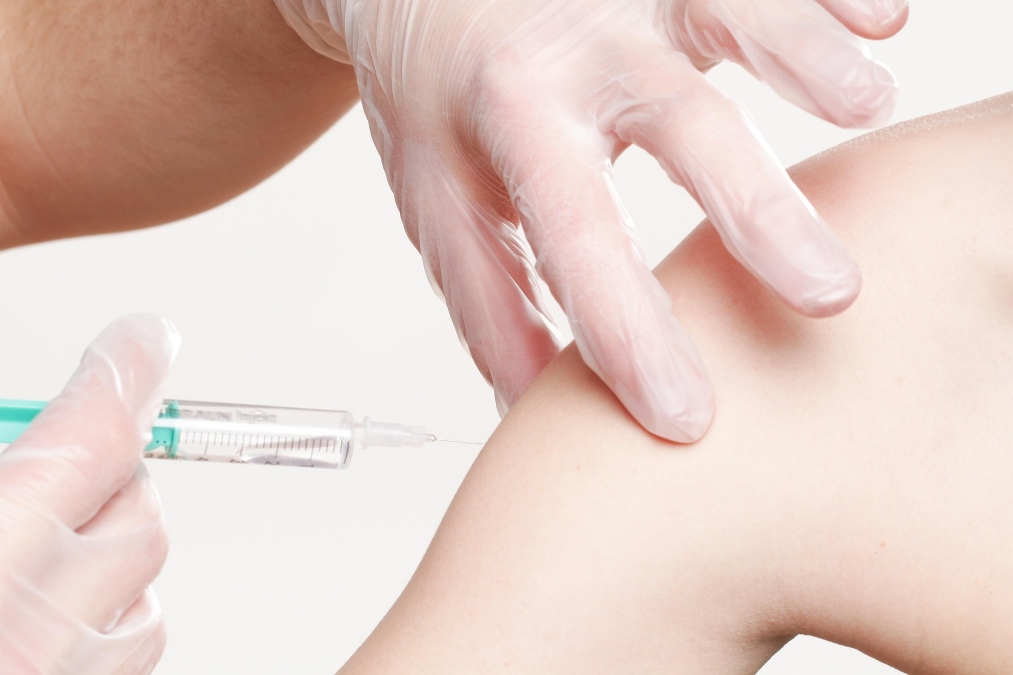
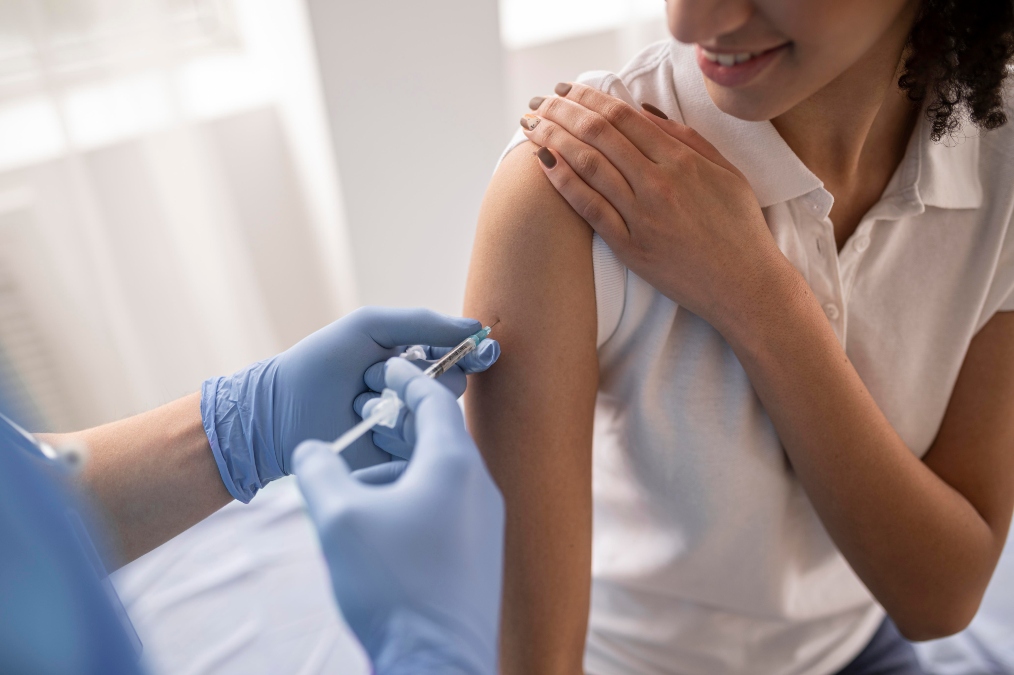
A Agência Nacional de Vigilância Sanitária (Anvisa) aprovou, nesta segunda-feira (12), o uso do lenacapavir injetável para a prevenção do HIV. O medicamento passa a integrar o conjunto de estratégias de profilaxia pré-exposição (PrEP), oferecendo uma alternativa de longa duração às pílulas orais tradicionais.

De acordo com a agência, o fármaco é indicado para adultos e adolescentes a partir de 12 anos, com peso mínimo de 35 quilos, que apresentem risco significativo de infecção. O uso exige testagem negativa para HIV antes do início do tratamento.
A decisão ocorre após avanços científicos e orientações internacionais. Em julho de 2025, a Organização Mundial da Saúde (OMS) recomendou o lenacapavir como opção adicional de PrEP, destacando sua eficácia e classificando-o como a melhor estratégia disponível após uma vacina. A OMS sugere a aplicação semestral, duas vezes ao ano, para ampliar a proteção em populações vulneráveis.
Em estudo publicado em 2024 na revista New England Journal of Medicine, o medicamento apresentou eficácia de 100% na prevenção do HIV entre mulheres participantes. Uma pesquisa complementar, conduzida no mesmo ano com 3.265 voluntários de diferentes gêneros, registrou apenas dois casos de infecção entre os usuários do antirretroviral.
Para Tedros Adhanom Ghebreyesus, diretor-geral da OMS, os dados reforçam o potencial do lenacapavir em um cenário global de estagnação dos esforços de prevenção. No último ano, 1,3 milhão de novas infecções foram notificadas em todo o mundo, segundo a organização.
Durante a 25ª Conferência Internacional sobre Aids, realizada em Munique, em 2024, a Gilead Sciences apresentou resultados que confirmaram uma eficácia geral de 100% na prevenção da infecção pelo HIV-1, predominante globalmente. O estudo, que acompanhou mais de 2 mil mulheres cisgênero em Uganda e na África do Sul, foi interrompido antecipadamente devido ao desempenho superior ao esperado.
Leia também: Anvisa aprova nova RDC que regulamenta o receituário eletrônico de medicamentos controlados
O Unaids afirmou recentemente que a chegada do medicamento representa um avanço importante para acelerar a resposta global contra a Aids e fortalecer as metas da Agenda 2030, que prevê a eliminação da doença como ameaça à saúde pública. Além do novo injetável, a OMS também passou a recomendar o uso ampliado de testes rápidos como estratégia para simplificar e acelerar o diagnóstico.
Fonte: CFF