
Nova Nota Técnica sobre testes rápidos é publicada pela Anvisa
No texto, a Agência reitera quais pré-requisitos devem ser seguidos para a execução dos testes e recomenda os de pesquisa de antígeno viral.

No texto, a Agência reitera quais pré-requisitos devem ser seguidos para a execução dos testes e recomenda os de pesquisa de antígeno viral.

O ensaio clínico foi autorizado pela Anvisa e já está sendo realizado desde julho nos Estados Unidos.
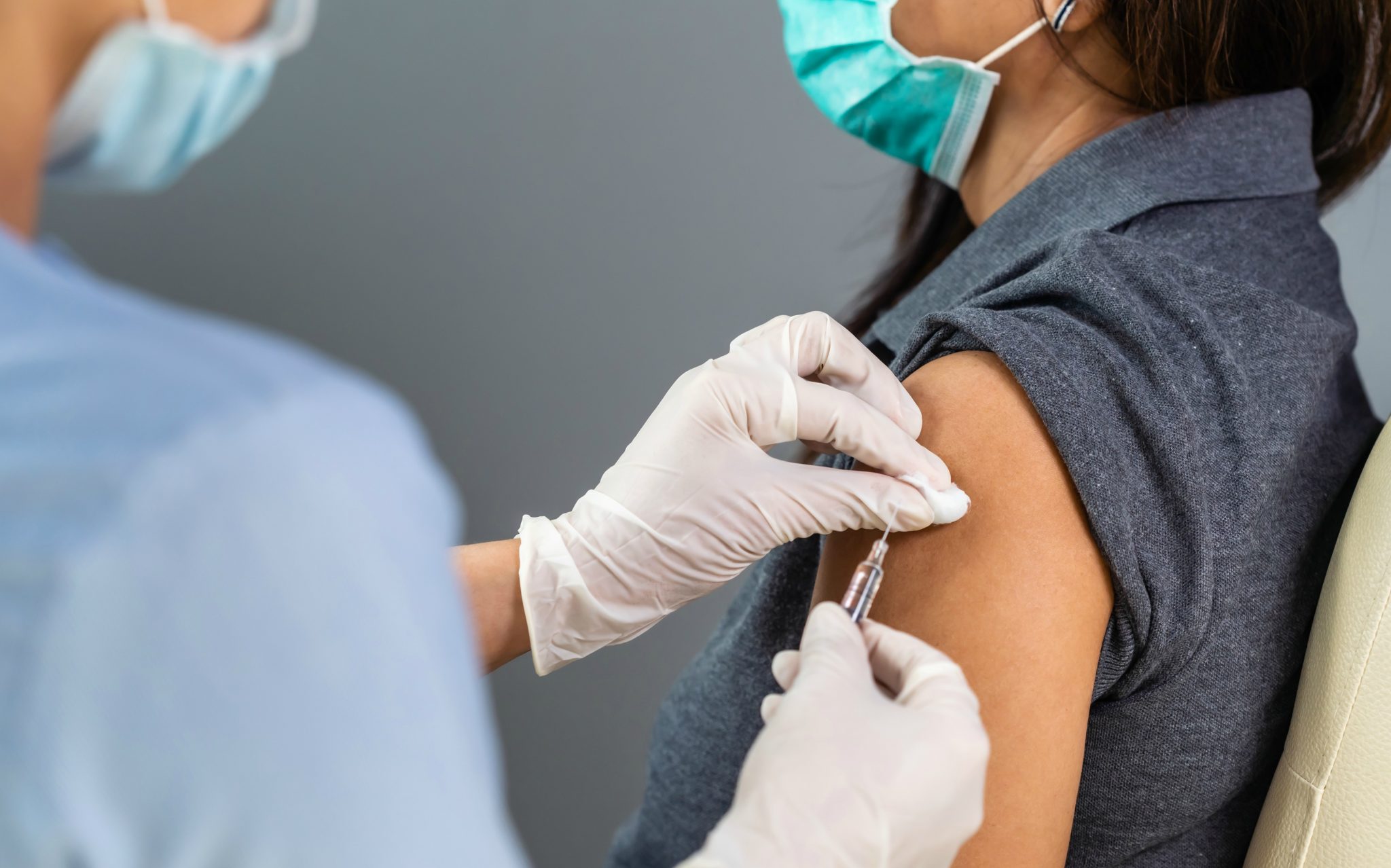
Como unidades de saúde, as farmácias estão preparadas para participar ativamente da imunização contra a Covid-19.
O projeto engloba mais de quatro mil farmácias para a aplicação das vacinas em 2021.

Pedido foi feito à Agência Europeia de Medicamentos, que poderá decidir sobre ambas as vacinas entre o fim de dezembro e meio de janeiro.
Segundo informações publicadas pelo governo russo, as primeiras pessoas foram vacinadas na semana passada.
Pedido de autorização para uso emergencial deve ser feito ainda hoje pela farmacêutica à FDA.

O medicamento ajuda no combate dos distúrbios de coagulação que afetam os vasos das pernas e dos pulmões.

A análise dos resultados dos estudos clínicos será feita continuamente. Medida vale apenas para vacinas contra a Covid-19.
Para notícias e ofertas exclusivas, digite seu e-mail abaixo.
Para notícias e ofertas exclusivas, digite seu e-mail abaixo.
Utilizamos cookies para garantir que você tenha a melhor experiência em nosso site. Se você continuar a usar este site, vamos assumir que você está feliz com isso.